Comparação entre Cr2O3 e SiO2 como marcadores na estimativa dos coeficientes de digestibilidade aparente de minerais em rações para tilápia do Nilo após extração ultra-sônica e quantificação por GFAAS
2 - UNESP/IBB/Botucatu
3 - UNESP/Botucatu
RESUMO -
Nos estudos de digestibilidade na nutrição animal, os marcadores externos são os mais utilizados, sendo o óxido de crômio (Cr2O3), o marcador que apresenta melhor aceitação. No entanto, as quantificações de Cr2O3 apresentam dificuldades nos procedimentos de preparo das amostras, uma vez que a mineralização é feita por aquecimento lento em blocos digestores utilizando-se mistura nítrico-perclórica, sendo os extratos resultantes, soluções ácidas contendo íons dicromato, espécie altamente tóxica. Além disso, há a problemática em decorrência das quantidades administradas e divergências quanto aos resultados de pesquisas, devido às variabilidades analíticas encontradas. Dessa forma, o uso de marcador naturalmente presente nas rações como a sílica (SiO2) seria uma alternativa ao uso do Cr2O3 em ensaios de digestibilidade e sua determinação em amostras de rações e fezes de peixes por espectrometria de absorção atômica em forno de grafite (GFAAS) apresenta-se como uma metodologia de estudo bastante promissora. Esta técnica permite a eliminação da etapa de mineralização ácida, principal problema pela metodologia clássica e redução no tempo das análises. Nesse contexto, o trabalho teve por objetivo otimizar os parâmetros analíticos envolvidos na quantificação de silício por GFAAS e posteriormente, comparar os coeficientes de digestibilidade de minerais em rações de tilápia do Nilo (submetidas previamente à extração ultra-sônica) obtidos com a utilização desses dois marcadores. Os resultados demonstraram que 5 ciclos de 60 s a 136 W foram suficientes para extração ultra-sônica dos analitos e dos marcadores. Já a comparação entre os coeficientes de digestibilidade, apesar de concordantes (P>0.05), sugerem que mais estudos sejam desenvolvidos com diferentes rações (matrizes) de diferentes espécies animais de forma a avaliar a reprodutibilidade na recuperação de SiO2, garantindo assim, que ele possa efetivamente ser uma alternativa ao uso de Cr2O3.
Comparison of Cr2O3 and SiO2 as dietary markers for estimation of minerals’ apparent digestibility coefficients in Nile tilapia feed after ultrasonic extraction and determination by GFAAS
ABSTRACT - In animal nutrition digestibility studies, the external markers are the most used, being chromium oxide (Cr2O3) that presents best acceptance. However, the quantifications of Cr2O3 present difficulties in samples’ pre-treatment, because the mineralization is done under slow heating in digestion blocks using nitric-perchloric mixture, that generates acid solutions containing dichromate ions, a highly toxic specie. In addition, there is a problem resulting from the administered quantities and divergences regarding researches results, due to the analytical variations. Thus, the use of a natural occurring marker in diets such as silicon oxide (SiO2) would be an alternative to the use of Cr2O3 in digestibility assays, and their determination in fish samples by graphite furnace atomic absorption spectrometry (GFAAS) represents a very promising methodology in animal nutrition studies. This technique allows the elimination of samples’ acid mineralization, the main problem by traditional methodology, and allows time reduction of analysis. Considering the aforementioned, the present work’s objective was to optimize the analytical parameters involved in silicon determination by GFAAS and to compare the minerals’ apparent digestibility coefficients (Fe, Zn, Ca, Mg and P) between these two markers in Nile tilapia feed (previously submitted to ultrasonic extraction). The results showed that 5 cycles of 60s and 136 W were sufficient for analytes-markers' ultrasound extraction. The comparison between markers, although in accordance (P>0.05), suggests that another studies should be carried out with different feed (matrices) of different animal species, in order to evaluate the reproducibility of SiO2 recovery, thus ensuring that it can effectively be an alternative to the use of Cr2O3.Introdução
Os animais possuem habilidades distintas para aproveitar os nutrientes e a energia contida nos alimentos, em decorrência de suas características morfológicas e fisiológicas. Assim, a avaliação do valor nutricional dos alimentos fica correlacionada à sua composição de nutrientes e à capacidade do animal em ingeri-los e absorvê-los. Nesse aspecto, o grau de aproveitamento do alimento pelo animal está atrelado à espécie, condições ambientais, quantidade e qualidade do nutriente, proporção relativa entre os nutrientes e aos processos tecnológicos a que o alimento foi submetido (ANDRIGUETTO, 2002). Para determinar a digestibilidade aparente de um ou mais nutrientes presentes em uma ração ou alimento, um dos métodos atualmente mais empregados é o uso de marcadores (método indireto ou coleta parcial de fezes), que se dividem em internos, quando ocorrem naturalmente nos alimentos (a exemplo do SiO2) e em externos (a exemplo do Cr2O3), quando são adicionados à dieta. Este último permite maior facilidade na condução dos ensaios, principalmente quando são feitos com peixes, já que a porcentagem da digestibilidade do nutriente pode ser avaliada sem a necessidade de determinar a quantidade de ração consumida e de fezes produzidas (RINGO, 1993).Revisão Bibliográfica
Nos estudos de digestibilidade na nutrição animal, os marcadores externos são os mais utilizados, sendo o óxido de crômio (Cr2O3), o marcador que apresenta melhor aceitação (HANLEY, 1987). A determinação da porcentagem de Cr2O3 e dos minerais nas fezes dos peixes permite estimar o coeficiente de digestibilidade aparente dos nutrientes metabolizados, comparando-se com a porcentagem desse óxido misturado inicialmente na ração (SILVA et al., 2006). No entanto, as quantificações do Cr2O3 nas rações e fezes apresentam dificuldades nos procedimentos de preparo das amostras, uma vez que a mineralização é feita por aquecimento lento em blocos digestores utilizando-se mistura nítrico-perclórica, sendo os extratos resultantes, soluções ácidas contendo íons dicromato (Cr2O72-), espécie altamente tóxica (SILVA et al., 2007; SALEH et al., 2013). Além disso, o uso de marcadores externos apresenta problemática em decorrência das grandes quantidades administradas para a obtenção de resultados analíticos adequados e divergências quanto aos resultados de pesquisas, devido às variabilidades analíticas encontradas (UDEN et al., 1980; KOZLOSKI et al., 1998). Dessa forma, o uso de marcadores naturalmente presentes nas rações como a sílica (SiO2), seria uma alternativa ao uso do Cr2O3, em decorrência desta não interferir no metabolismo digestório do animal, não ser absorvida ou metabolizada, além de ser atóxica (KABIR et al., 1998). Portanto, o desenvolvimento de novas metodologias que permitam a quantificação segura dos nutrientes e dos compostos utilizados como marcadores nos estudos de digestibilidade aparente na nutrição animal torna-se fundamental. Neste contexto, a avaliação da sílica como marcador interno em estudos de digestibilidade e a determinação desta nas amostras de rações e fezes de tilápia do Nilo (Oreochromis niloticus) após extração ultra-sônica e determinação por GFAAS, apresenta-se como uma metodologia de estudo bastante promissora, sendo o objetivo principal do presente estudo, uma vez que apresenta vantagens tais como, eliminação da etapa de mineralização das amostras, redução do tempo das determinações analíticas e não geração de resíduos tóxicos, que possam comprometer a saúde do analista e/ou contaminar o meio ambiente.Materiais e Métodos
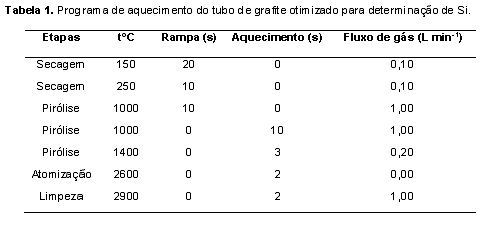
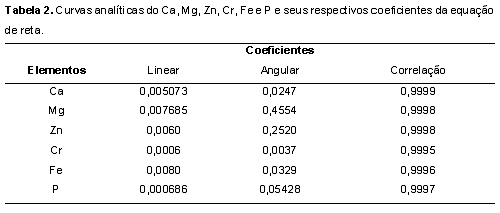
Reagentes e soluções Água ultrapura (18,2 MΩ cm-1) obtida pelo sistema Elga, modelo Purelab Ultra (Veolia Water Technologies, UK) foi utilizada no preparo das soluções padrão e das amostras. As soluções padrão de silício (Si) foram preparadas por diluições de padrão titrisol (Merck, Darmstadt, Germany) e as soluções dos concomitantes e analitos foram preparadas a partir de reagentes de pureza espectroscópica (Johnson & Matthey, Hertfordshire, UK). As demais soluções utilizadas, incluindo as soluções ácidas concentradas utilizadas nas mineralizações das amostras foram todas de grau analítico. Todas as soluções foram estocadas em frascos de polipropileno. Todos os frascos para estocagem de amostras, soluções padrão e vidrarias foram lavados com ácido nítrico 10% v/v por 24 h, em seguida, com água ultrapura e secos por jatos de ar puro antes de sua utilização. Instrumentação analítica Para secagem das amostras utilizou-se estufa de circulação forçada de ar (Tecnal, modelo TE-394/1, Piracicaba, SP, Brasil) e na mineralização ácida das amostras, blocos digestores (Marconi, modelo MA-447/6/100, Piracicaba, SP, Brasil) com capacidade para 6 balões de 100 mL de fundo redondo (tipo Kjeldahl). Na extração por ultrassom dos analitos utilizou-se desruptor de células ultra-sônico (UNIQUE, modelo USC-DC, Campinas, SP, Brasil) com sonda de titânio de 3 mm. Ultracentrífuga (Hettich Lab., modelo Universal-320R, Tuttlingen, Germany) foi utilizada para separação da fração sólida remanescente dos extratos submetidos à extração ultra-sônica. Na determinação dos íons metálicos foi utilizado espectrômetro de absorção atômica (Shimadzu, modelo AA-6800, Tokyo, Japão) com módulo de chama (FAAS) e forno de grafite (GFAAS), equipado com corretor de absorção de fundo (lâmpada de deutério) e amostrador automático (ASC-6100). Lâmpadas de cátodo oco de Ca, Mg, Fe, Zn, Si e Cr foram utilizadas, seguindo as recomendações do fabricante (AAS COOKBOOK, 2000). Para determinação de P foi utilizado espectrofotômetro UV-Vis (Thermo Spectronic, modelo Genesys 6, Madison, USA) Preparo das amostras As amostras de rações e fezes de peixes provenientes de ensaios realizados pelo grupo de pesquisa do Laboratório de Nutrição de Peixes da FMVZ/UNESP/Botucatu foram secas a 50oC em estufa de circulação forçada de ar por 48 horas e submetidas à moagem. Dessa forma, uma massa de aproximadamente 1,0 g da amostra foi moída utilizando moinho criogênico (SPEX SamplePrep Geno/Grinder, modelo 2010, Metuchen, USA) regulado para 4 ciclos de 6 min em 1000 rpm de rotação a -196oC. Este procedimento permitiu a obtenção de partículas com granulometria menor que 60 micrômetros (ZANOTTO & BELLAVER, 1996). Nesses ensaios, 0,1% de óxido de crômio foi adicionado às rações experimentais, conforme estudos preliminares (FURUKAWA & TSUKUHARA, 1966; AUSTRENG, 1978). Outra porção das amostras foi mineralizada utilizando blocos digestores. Para isso, 100 mg das amostras de rações e fezes foram transferidos para balões de borosilicato (tipo Kjeldahl) de 100 mL, onde foram adicionadas alíquotas na proporção de 3,0 mL de solução concentrada de ácido nítrico 65% Merck e, quando necessário, acrescentou-se peróxido de hidrogênio 30% m/m para auxiliar na completa oxidação da matéria orgânica. Posteriormente, alíquota de 1 mL de ácido perclórico 70% Merck foi adicionada para que os íons Cr (III) fossem oxidados a Cr (VI). Os extratos ácidos obtidos após total mineralização das amostras foram transferidos por meio de lavagens sucessivas com água ultrapura para balão volumétrico de 50 mL. Em cada mineralização foi preparado um branco que continha todos os reagentes utilizados na mineralização ácida das amostras, exceto a amostra em questão. Preparo da curva analítica de Si (análise por GFAAS) Para determinação do Si foi utilizado espectrômetro de absorção atômica Shimadzu modelo AA-6800, equipado com corretor de absorção de fundo (lâmpada de deutério), plataforma integrada e amostrador automático (ASC-6100). Foi utilizada lâmpada de catodo oco de Si, operada em 10 mA de corrente e tubo de plataforma, de aquecimento transversal, com o intuito de avaliar o comportamento eletrotérmico do Si em relação aos sinais de absorbância. O comprimento de onda utilizado foi de 251,78 nm e a resolução espectral foi de 0,5 nm. O argônio foi utilizado como gás inerte, mantendo um fluxo constante durante todo o programa de aquecimento, exceto na etapa de atomização, na qual o fluxo de gás foi interrompido. Os sinais de absorbância foram medidos em área de pico. Inicialmente, suspensões padrão contendo de 50 a 250 microgramas por litro de Si foram preparadas utilizando 50 microgramas de amido desidratado, ingrediente isento do analito estudado e alíquotas de 5 microlitros de solução estoque de Si de 1 mg L-1, 100 microlitros de solução de W0 a 1000 mg L-1, 200 microlitros de solução de Pd0 a 1000 mg L-1, 500 microlitros de solução a 0,01% de Triton X-100 e 14,2 microlitros de água ultra-pura para completar o volume em 20 microlitros. Em seguida, também foram testados os sinais de absorbância de Si utilizando soluções padrão aquosas contendo de 0 a 80 microgramas por litro de Si preparadas utilizando solução estoque contendo 100 microgramas por litro de Si, adotando volumes de 4, 8, 12, 16 e 20 microlitros de solução padrão de Si a serem injetados no interior do tubo de grafite pela micropipeta do auto-amostrador juntamente com 16, 12, 8, 4 e 0 microlitros de água deionizada, respectivamente, de forma que o volume final de injeção fosse 20 microlitros. As medidas foram feitas em triplicata. O programa de aquecimento utilizado nesse estudo encontra-se detalhado na Tabela 1. Preparo de soluções padrão e curvas analíticas para Ca, Mg, Zn, Cr, Fe e P As soluções padrão aquosas dos minerais foram preparadas a partir de diluições de padrões titrisol (Merck) contendo 1000 mg L-1 de cada analito. As faixas ótimas de concentração das curvas analíticas utilizadas foram: Ca (0,5; 1,0; 2,0; 4,0 e 5,0 mg L-1), Mg (0,1; 0,2; 0,4; 0,8 e 1,0 mg L-1), Zn (0,2; 0,4; 0,6; 0,8 e 1,0 mg L-1), Cr (1,0; 2,0; 4,0; 6,0; 8,0 mg L-1) e Fe (1,0; 2,0; 4,0; 6,0; 8,0 mg L-1). A Tabela 2 apresenta as curvas analíticas obtidas para os minerais com seus respectivos coeficientes linear, angular e de correlação e as determinações foram feitas por espectrometria de absorção atômica por chama (FAAS) estando as condições operacionais sumarizadas na Tabela 3. No preparo das soluções padrão aquosas de Ca e Mg foi preparada solução de lantânio 50 g L-1, sendo alíquota de 10 mL transferida para cada frasco dos padrões, de forma a evitar a formação de compostos insolúveis com o cálcio. As determinações de fósforo por espectrofotometria UV-Vis foram realizadas segundo o método do ácido vanadomolíbdico fosfórico (método amarelo), em comprimento de onda ajustado de máxima absorção a 420 nm. As condições operacionais utilizadas foram as descritas no manual do fabricante do equipamento Thermo Spectronic, modelo Genesis 6. No preparo da curva analítica para determinação do P preparou-se solução estoque de P a 38,72 mg L-1 a partir de solução de KH2PO4 a 0,00125 mol L-1. Assim, a faixa de concentração dos padrões de P obtida foi, respectivamente, de 1,55; 3,10; 4,65; 6,97 e 9,29 mg L-1. Para cada curva analítica foi preparado um branco que continha todos os componentes das soluções padrão com exceção do analito de interesse. Cálculos dos coeficientes de digestibilidade aparente O coeficiente de digestibilidade aparente (CDa) é dado pela relação entre a porcentagem do marcador presente inicialmente na ração (%Mr) e o obtido posteriormente nas fezes (%Mf) e, a porcentagem do nutriente obtido nas fezes (Nf) pela porcentagem do nutriente inicialmente presente na ração (Nr), nos permitindo, portanto, saber quanto do nutriente foi absorvido pelo animal, considerando a diferença do que inicialmente foi administrado na ração e do que foi obtido nas fezes (SHAHAT, 1993), ou seja, a fração do alimento que realmente foi aproveitada pelo animal. Após a obtenção dos valores em porcentagem dos minerais e das porcentagens de Si e Cr para o cálculo dos marcadores na forma de óxido (o interno: SiO2 e o externo: Cr2O3) foram feitos os cálculos dos coeficientes de digestibilidade aparente (CDa), considerando a equação matemática: CDa = 100 – [100 x (%Mr / %Mf) x (%Nf / %Nr)] proposta por MAYNARD & LOOSLI (1956) e em seguida, procedeu-se à comparação entre os resultados obtidos dos minerais utilizando SiO2, como marcador interno e os resultados obtidos utilizando Cr2O3, como marcador externo. Análise estatística Os resultados foram submetidos à análise de variância (ANOVA) utilizando o procedimento PROC GLM do SAS (2008), sendo as médias comparadas pelo teste F (P<0,05).Resultados e Discussão
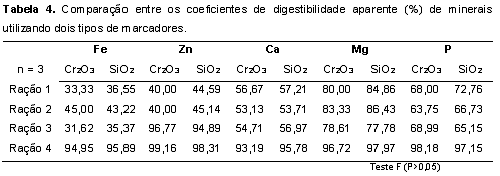
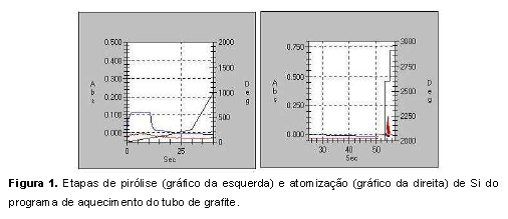
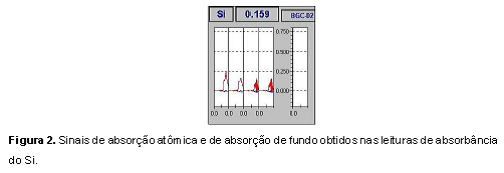
Otimização das condições instrumentais Nas determinações de Si por GFAAS, a obtenção de resultados analíticos exatos e reprodutíveis dependem da otimização das temperaturas de pirólise e atomização do analito em suspensão presente na amostra (ALEIXO et al., 2000; MINAMI et al., 1997). Conforme fornecido na Tabela 1, utilizando temperaturas de 1400°C e 2600°C foi possível obter a total pirólise dos concomitantes da amostra e a atomização do Si, obtendo bons sinais de absorbância, conforme demonstram os gráficos da Figura 1. Outro parâmetro avaliado na otimização das condições instrumentais foi o perfil do sinal atômico transiente. Este parâmetro permitiu avaliar a cinética de atomização do analito, em função do tempo de aparecimento do sinal e do tempo de retorno à linha de base. A Figura 2 mostra os sinais de absorção atômica (em vermelho) e de absorção de fundo (em azul) obtidos utilizando os parâmetros otimizados descritos anteriormente. Pode-se observar que todos os sinais de absorbância mostraram uma certa semelhança, apresentam-se bem definidos e homogêneos, com tempos de aparecimento e retorno à linha de base bem próximos. Esse comportamento comprova a eficiência das temperaturas de pirólise e atomização utilizadas. O caráter refratário do Si permitiu a utilização de altas temperaturas de pirólise, sem a necessidade de utilização de modificador químico para estabilizá-lo termicamente. Por esse motivo, os melhores resultados foram obtidos sem a utilização de modificadores químicos permanentes (como o Pd0 e o W0 utilizados em testes preliminares), ressaltando ainda que no caso do W0, houve influência negativa no processo de atomização do Si, em decorrência do alto ponto de ebulição que este possui (5900°C), que ao formar ligação metálica com o Si provocou aumento significativo na temperatura de atomização, bem acima dos 2600°C necessários nesse processo. Além disso, o filme de carbeto de tungstênio formado na superfície do tubo de grafite ao interagir com a nuvem atômica de Si durante a etapa de atomização acarretou a diminuição do número de átomos de silício livres e na forma elementar, causando por consequência, a diminuição dos sinais de absorbância medidos. Dessa forma, optou-se por trabalhar na ausência de modificadores químicos e utilizar soluções padrão aquosas, uma vez que o Si é um elemento com características refratárias. Com essas otimizações foi possível obter curvas analíticas com excelentes coeficientes de correlação linear. Obtenção das curvas analíticas dos padrões de Si por GFAAS Após a otimização dos parâmetros instrumentais (temperaturas de pirólise, atomização e sinais transientes de absorção atômica e de fundo) foram construídas curvas analíticas utilizando-se suspensões padrão (faixa de concentração: 50, 100, 150, 200 e 250 microgramas por litro; equação de reta: Abssuspensão = 0,002785 x CSi + 0,07751; r = 0,9948) e padrões aquosos (faixa de concentração: 0, 20, 40, 60 e 80 microgramas por litro; Absaquoso = 0,00304 x CSi + 0,01724; r = 0,9993). Analisando as curvas analíticas obtidas observou-se que a curva utilizada com padrões aquosos apresentou melhor ajuste, o que foi comprovado em função dos coeficientes de correlação obtidos em ambos os casos (rsuspensão = 0,9948; raquoso = 0,9993). Dessa forma, a curva analítica com padrões aquosos foi utilizada nas quantificações posteriores de Si em amostras de rações e fezes de peixes para comparação dos coeficientes de digestibilidade. Os valores dos limites de detecção (LOD) e de quantificação (LOQ) calculados considerando os desvios padrão de vinte leituras do branco da curva analítica aquosa e o valor da inclinação da reta obtida (LOD=3xsd/slope e LOQ=10xsd/slope) (CURRIE, 1999) foram de LOD: 2,2 microgramas por litro e LOQ: 7,2 microgramas por litro. Aplicação do método de extração por ultrassom das amostras As otimizações do tempo e potência de sonificação das amostras (ração e fezes) foram obtidos variando-se a agitação ultra-sônica nos tempos de 5, 10, 20, 40 e 60 s e nas potências 17, 34, 68, 136 e 204 W, respectivamente. Em cada tempo foram utilizados cinco ciclos de agitação. As ondas ultra-sônicas além de favorecerem a homogeneidade da suspensão, promoveram a extração dos analitos da matriz e contribuíram para redução da granulometria da amostra devido à atuação das ondas sobre as moléculas orgânicas, provocando a quebra da ligação do metal com essas moléculas e liberando-o para a suspensão (SALEH et al., 2015). Os resultados demonstraram que 5 ciclos de 60 segundos de agitação ultra-sônica, utilizando 40% da potência máxima de trabalho (136 W) foram suficientes para obter os melhores sinais de absorbância quando se analisaram o Ca, Mg, Fe, P e Zn nos extratos obtidos. A substituição da mineralização ácida pela extração por ultrassom mostrou-se mais vantajosa em razão da diminuição do tempo de preparo das amostras, não utilização de soluções ácidas concentradas e nem geração de resíduos tóxicos prejudiciais ao analista e ao meio ambiente, diminuição do tempo total das determinações analíticas, além de gerar resultados concordantes com a técnica clássica de mineralização ácida (nítrico-perclórica). Comparação entre os coeficientes de digestibilidade aparente Podemos observar pela Tabela 4 que apesar de ter sido observada certa variação entre os dados dos marcadores, eles foram concordantes (P>0,05). De maneira geral, os CDa obtidos utilizando a sílica mostraram-se maiores que os obtidos com o óxido de crômio, o que provavelmente tenha sido em razão da sílica ter apresentado taxa de passagem mais rápida pelo trato gastro-intestinal das tilápias em comparação com a taxa de passagem do óxido de crômio. Esses resultados corroboram os obtidos por LEAVITT (1983) em estudo com lagosta americana, bem como com os de TACON & RODRIGUES (1984) em estudo com truta arco-íris. Em razão dessa maior taxa de passagem, pode ser que a equação matemática utilizada não seja adequada para marcador interno que apresenta concentrações variáveis dependendo da fonte alimentar. Portanto, os resultados apresentados reforçam a necessidade do desenvolvimento de estudos para propor um modelo matemático que permita correlacionar de forma mais segura diferentes tipos de marcadores utilizados em experimentos de digestibilidade de nutrientes na nutrição de peixes.Conclusões
A metodologia proposta de extração por ultrassom de Ca, Mg, Fe e Zn de amostras de rações e fezes de peixes e posterior quantificação por FAAS e do P, por espectrofotometria UV-Vis, obteve resultados equivalentes à mineralização das amostras em blocos digestores, apresentando ainda a vantagem de não gerar resíduos tóxicos que pudessem comprometer a saúde da analista e contaminar o meio ambiente. Além disso, com a técnica de extração ultra-sônica, o tempo das determinações analíticas foi reduzido consideravelmente. Em relação à utilização da sílica como marcador interno, os resultados obtidos sugerem que mais estudos devam ser desenvolvidos em amostras de diferentes espécies animais, contemplando os demais nutrientes comumente adicionados às rações, de forma a avaliar a reprodutibilidade na recuperação deste marcador, garantindo assim, que ele possa efetivamente ser uma alternativa à utilização do óxido de crômio.Gráficos e Tabelas