
Uso da espectroscopia no infravermelho por transformada de Fourier com reflectância total atenuada (FTIR-ATR) como teste de triagem de ivermectina em leite
2 - Universidade Estadual do Sudoeste da Bahia
3 - Universidade Estadual do Sudoeste da Bahia
4 - Universidade Estadual do Sudoeste da Bahia
5 - Universidade Estadual do Sudoeste da Bahia
6 - Universidade Estadual do Sudoeste da Bahia
7 - Universidade Estadual do Sudoeste da Bahia
8 - Universidade Estadual do Sudoeste da Bahia
RESUMO -
É necessário o aumento do número de amostras coletadas oficialmente para avaliar a presença de Ivermectina (I) em leite cru, o que torna importante o desenvolvimento de testes rápidos, ou testes de triagem. Avaliamos a espectroscopia de infravermelho por transformada de Fourier com reflectância total atenuada (FTIR-ATR), como teste de triagem de Ivermectina em leite. Foram coletados 500 mL de leite de 10 vacas em três períodos com intervalo de 8 dias. Às amostras de leite por vaca e por período foi acrescentada a Ivermectina nas seguintes concentrações: 0, 2, 4, 6, 8, 10, 12, 14, 16, 18 e 20 µg/L (n=330/vaca). As respostas foram analisadas por meio do uso de Análise de Componentes Principais (ACP). Os componentes principais agruparam as amostras de leite puro, dos leites adulterados e de Ivermectina indicando que o método foi capaz de identificar a adulteração, mesmo nas menores concentrações. O método de FTIR-ATR pode ser usado como teste de triagem de Ivermectinas me leite.
Attenuated total reflectance Fourier transform infrared spectroscopy (ATR-FTIR) as a ivermectin screening test in milk
ABSTRACT - It is necessary the increase in the samples numbers officially collected to evaluate the presence of Ivermectin (I) in raw milk. For this, a screening tests should be developed. The Fourier transform infrared spectroscopy (FTIR) attenuated total reflectance (ATR) spectroscopy, coupled with chemometrics methods have been applied to detect the Ivermectin and develop a screening test. Milk samples (500 mL) from 10 cows in the 3 periods were collected. From this, milk aliquots from each cow and period were separated for add the Ivermectin standard as follow: 0, 2, 4, 6, 8, 10, 12, 14, 16, 18 e 20 µg/L (n=330/cow). Principal Components Analysis was used (PCA). The principal components grouped the samples (pure milk, adulterated milks and Ivermectin) indicating that the method was able to identify adulteration, even in the lowest concentrations. The FTIR-ATR can be used as screening test for evaluate Ivermectin in milk samples.Introdução
O uso de medicamentos veterinários em animais de lactação vem sendo realizado em todo mundo com a finalidade de combater doenças ou aumentar a produtividade e esses medicamentos podem ser excretados, entre outras formas, por meio do leite, exemplo da Ivermectina que é utilizada no combate a endo e ectoparasitas. A utilização de Ivermectina ocorre, muitas vezes, sem o controle necessário, o que gera preocupação em relação aos resíduos que podem ocorrer nos alimentos oriundos dos animais nos quais foi administrada.
O controle de Ivermectina no leite é feita por meio de Cromatografia líquida de alta eficiência, técnica de alto custo e laboriosa, nesse sentido, este trabalho propõe uma nova técnica que sirva como teste de triagem. Assim, o objetivo do trabalho foi o desenvolvimento e validação do uso de espectroscopia no infravermelho médio por transformada de Fourier na detecção de resíduos de Ivermectinas em leite.Revisão Bibliográfica
A Ivermectina é um medicamento que faz parte do grupo das Lactonas Macrocíclicas, é composta por, no mínimo 80% de 22,23-diidroavermectina B1a e menos de 20 % de 22, 23-diidroavermectina B1b (Vercruysse e Rew, 2002).
A detecção e quantificação da Ivermectina em leite é feita por cromatografia líquida de alta eficiência (Cerkvenik-Flajs et al., 2010; Escribano et al., 2012), técnica laboriosa e de alto custo. Em função disso, a avaliação oficial da presença de medicamentos veterinários é feita em número pequeno (Brasil, 2003). Buscando agilidade no processo, testes de triagem para Lactonas Macrocíclicas são buscados em todo o mundo, contudo usando técnicas também laboriosas (Jeong et al., 2012; Wei et al., 2015).
No Brasil, o limite máximo de resíduo de Ivermectina é de 10 µg*mL-1 e estudos indicam presença de Ivermectina variando entre 0%-52% das amostras (Lobato et al., 2006; Cerqueira et al., 2014; Brasil, 2015). O controle oficial (n=217) não encontrou amostras com resíduos (Brasil, 2015), no entanto, Lobato et al. (2006) detectaram resíduos (n=168), mas, com amostras dentro do limite legal e Cerqueira et al. (2014) indicam 6% das amostras em não conformidade (n=83). É certo que o local da amostragem, assim como, o número de amostras pode interferir.Materiais e Métodos
Obtenção e preparo das amostras
Para a realização do experimento, foram utilizadas amostras de leite puro, padrão de Ivermectina e leite adulterado com Ivermectina nas concentrações de:0, 2, 4, 6, 8, 10, 12, 14, 16, 18 e 20 µg/L de leite. Após a obtenção, as amostras de leite foram liofilizadas para posterior análise.
Análise espectrofotométrica
Os espectros das amostras foram determinados com o uso da espectroscopia por reflectância total atenuada acoplada, na região do infravermelho médio 4000-400 cm-1 por transformada de Fourier (ATR-FTIR), em equipamento Cary 630 (Agilent, Santa Clara, USA). Os dados foram obtidos com o uso do software Microlab e o Resolution Pro (Agilent, Santa Clara, USA).
Análise de Componentes Principais
Os resultados das análises foram organizados em um conjunto de dados que foram padronizados a partir do desvio padrão e do coeficiente de variação
Após o tratamento dos dados e obtenção das médias padronizadas, as variáveis Y foram utilizadas para a ordenação de um novo sistema de coordenadas com eixos ortogonais
A partir desse sistema, foram obtidos os Componentes Principais (CP’s) em ordem decrescente de variância, em que, o CPi explicou a maior variação dos dados quando comparado a CPi+1 e assim sucessivamente. Essa ordenação possibilitou a redução do número de variáveis, inicialmente igual a 45. Para a seleção dos CP’s, foram utilizados os critérios de Kaiser, que seleciona os primeiros CP’s que acumulam percentual de variância superior a 70% e autovalor maior que 1 (JOLLIFFE, 1972) e Mardia et al. (1979) que torna passível de descarte variáveis de forte correlação com CP’s de menor autovalor (variância). Associados à estes critérios, definimos que variáveis seriam excluídas em função da classificação das amostras pelos CP’s.Resultados e Discussão
Análise espectrofotométrica
A partir da análise com FTIR, foram obtidos os espectros das amostras, nos quais foram observadas 29 picos nos espectros da Ivermectina e 16 picos nos espectros do leite.
Análise de Componentes Principais (ACP)
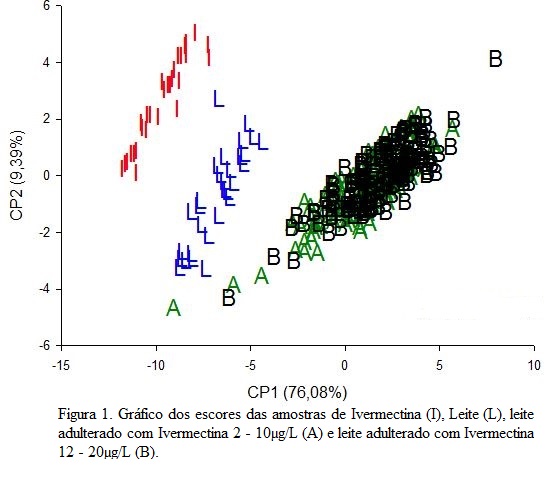
Para a ACP, as amostras foram agrupadas em: leite adulterado de 2-10 µg/L (A), leite adulterado de 12-20 µg/L (B), leite puro (L) e Ivermectina (I).
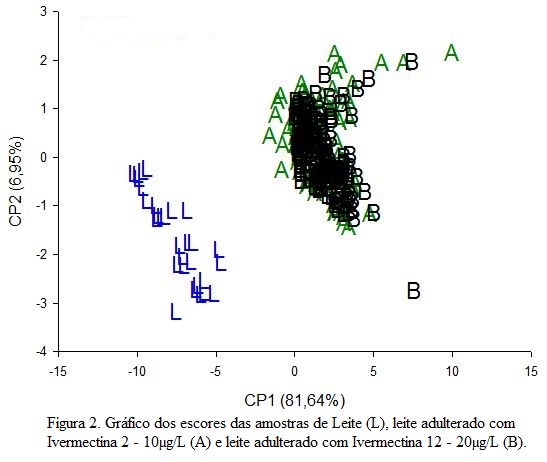
A partir da análise de componentes principais, verificou-se que, para todas as análises o CP1 e CP2 explicaram maior percentual da variância entre as amostras para todas as análises. Dessa forma, foi avaliado o comportamento da I, L e os leites adulterados (leite A e leite B). O resultado deixou claro a separação das amostras, agrupando-as de acordo com sua origem, Ivermectina, leite ou leite adulterado (Figura 1). No entanto, o objetivo com este estudo foi avaliar, por meio de ACP, o agrupamento de amostras de leite contaminado com Ivermectina ou não e, para isso, foram estudadas apenas amostras de leite (adulterado ou não). Os resultados foram expressivos, e demonstraram a separação das amostras de leite puro do leite contaminado (Figura 2).
Atendendo aos critérios pré-selecionados, 16 variáveis apresentaram alta correlação com CP1 ou CP2 e foram determinantes pra a separação das amostras. As variáveis obtidas nesta análise estão relacionadas a números de onda onde ocorrem vibrações moleculares características de Ivermectina, que são: 3450, 2963, 2934, 2887, 1676, 1457, 1380, 1340, 1312, 1065, 1046, 900, 832, 786, 760 e 736 cm-1. Isto indica que, como a análise foi realizada por meio de matriz de variância e covariância e o padrão da matriz estava relacionada ao espectro do leite, as variações nessa matriz ocorreram em função da presença de Ivermectina.
Estes resultados indicam a possibilidade do uso FTIR como teste de triagem para detecção de Ivermectina em leite, auxiliando no aumento do número de amostras que podem ser avaliadas.
Conclusões
A espectroscopia de infravermelho médio por transformada de Fourier pode ser usada para teste de triagem de Ivermectina em leite.
Gráficos e Tabelas
Referências
JOLLIFFE, I. T. Discarding variables in a principal component analysis - I: artificial data. Applied Statistics, Londres, v. 21, n. 2, p. 160-173, 1972.
MARDIA, K. V.; KENT, J. T.; BIBBY, J. M. Multivariate analysis. London: Academic, 1979. 520 p
BRASIL, Ministério da Agricultura, Pecuária e Abastecimento. Portaria SDA No 22, de 07 de Abril de 2015. Publicada no Diário Oficial da União – Seção 01 de 10/04/2015).
BRASIL. Programa Nacional de Análise de Resíduos de Medicamentos Veterinários em Alimentos Expostos ao Consumo – PAMVet. 2003, 9 p.
CERKVENIK-FLAJS, V.; MILCINSKI, L.; SUSSINGER, A.; HODOSCEK, L.; DANAHER, M.; ANTONIC, J. Trace analysis of endectocides in milk by high performance liquid chromatography with fluorescence detection. Analytica Chimica Acta 663 (2010) 165–171.
CERQUEIRA, M.M.O.P.; SOUZA, F.N.; CUNHA, A.F.; PICININ, L.C.A.; LEITE, M.O., PENNA, C.F.A.M.; SOUZA, M.R.; FONSECA, L.M. Detection of antimicrobial and anthelmintic residues in bulk tank milk from four different mesoregions of Minas Gerais State – Brazil. Arq. Bras. Med. Vet. Zootec., v.66, n.2, p.621-625, 2014. http://dx.doi.org/10.1590/1678-41627274
ESCRIBANO, M.; SAN ANDRÉS, M. I.; LUCAS, J. J. CANGA, A. G. . Current Ivermectin Residue Depletion in Food Producing Species and its Presence in Animal Foodstuffs With a View to Human Safety. Pharmaceutical Biotechnology, 2012, 13, 987-998.
JEONG, I. S.; KWAK, B.M.; AHN, J. H.; JEONG, S. H. Determination of pesticide residues in milk using a QuEChERS-based method developed by response surface methodology. Food Chem. 133:473–481. 2012.
LOBATO, L.; RATH, S.; REYES, F. G. R. Occurrence of ivermectin in bovine milk from the Brazilian retail market Food Additives and Contaminants, July 2006; 23(7): 668–673
VERCRUYSSE J.; REW, R. S. Macrocyclic lactones in antiparasitic therapy. CAB International, Wallingford, UK, 2002.
WEI, H.; TAO, Y.; CHEN, D.; XIE, S.; PAN, Y.; LIU, Z.; HUANG, L.; YUANA, Z. Development and validation of a multi-residue screening method for veterinary drugs, their metabolites and pesticides in meat using liquid chromatography-tandem mass spectrometry. Food Additives & Contaminants: Part A, 2015. Vol. 32, No. 5, 686–701, http://dx.doi.org/10.1080/19440049.2015.1008588.


